

近年来,广东省致力于发展生物医药与健康战略性支柱产业集群,珠三角地区聚集了大量研发型生物技术公司。根据2022年发布的《广州生物医药企业创新发展报告》,2021年,广州生物医药企业数目为6400多家,位居全国第三。同时,多家药企如华润三九、香雪制药将总部设立于广东,百济神州也已在广东建立了生产基地。越来越多的医药企业聚集与发展,体现了医药产业持续向好的发展态势。
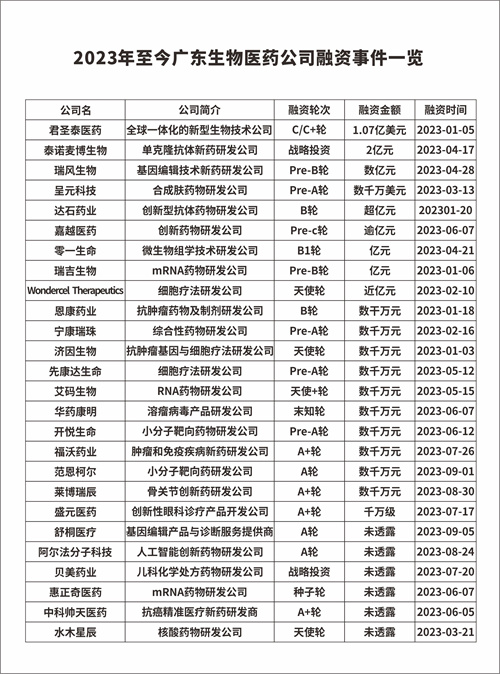
据不完全统计,2023年至今,共有26家生物医药公司获得融资,金额总计超20亿元。值得关注的亮点包括:
早期融资事件数超八成:未知轮外,26家生物医药公司中21家完成了B轮及以前的早期融资,总金额达到近10亿元。
1月出现融资高峰:1月融资事件数为5起,总金额达到近1.4亿美元,均为2023年至今的单月最高值。最高融资额来自于君圣泰医药的1.07亿美元C/C+轮融资。君圣泰医药(HighTideTherapeutics, Inc.)是一家全球一体化的新型生物技术公司,专注代谢性疾病、消化系统疾病等领域的重大未满足临床需求。公司立足源头创新,以患者的综合临床获益和整体健康改善为目标,开发First-in-Class、多功能、多靶点、多适应症的原创新药。
9家公司融资超亿元:超亿元融资公司中4家来自深圳,3家来自广州,其余2家分别来自珠海和中山。
半数公司主要研发新型疗法技术:26家或融资公司中13家公司关注新型疗法领域,包括泰诺麦博生物、瑞风生物、呈元科技等公司;涉及领域包含新型抗体、基因与细胞疗法、多肽、RNA药物、微生物组学、溶瘤病毒。
# 君圣泰医药:全球一体化的新型生物技术公司
1月5日,君圣泰医药(HighTideTherapeutics, Inc.)宣布完成 1.07 亿美元C/C+轮融资。本轮融资由国开金融及广东国资管理的广东中医药大健康基金领投,越秀产业基金、昱烽晟泰基金旗下百亿资本及相关企业参与投资。 本轮募集资金将用于推进君圣泰在研管线的多项临床中后期全球开发、商业化和商务拓展。
9月8日,据CDE官网,君圣泰医药HTD1801胶囊获批临床,拟开展治疗非酒精性脂肪性肝炎(NASH)的研究。
5月15日,君圣泰医药(HighTide Therapeutics, Inc.)宣布其核心产品HTD1801在针对2型糖尿病(T2DM)患者的2期临床试验中达到主要终点以及多个重要次要终点。数据显示,与安慰剂组相比,HTD1801治疗组达到优效且有临床意义的糖化血红蛋白(HbA1c)改善,且安全性和耐受性与安慰剂组相似。公开资料显示,HTD1801是君圣泰医药的核心产品。君圣泰医药主要产品有: 一个是NASH:2a期临床研究已达到首要终点及多个关键次要终点,2b期临床试验已启动,该产品已获得美国FDA快速通道资格认定,是NASH领域首个获得该认定的中国原创新药;第二个是T2DM:2期临床试验已完成 ,3期临床研究即将启动,2期研究结果显示核心产品可显著降低受试者的糖化血红蛋白水平和血糖水平,同时可显著改善肝功能相关生物标记物,实现“糖肝共治”,且对于肝功能异常的受试者,改善作用更加明显;第三个是PSC和原发性胆汁性胆管炎(PBC):已完成2期临床试验,试验结果达到了首要终点及关键次要终点,PSC已获得美国FDA孤儿药资格认证和快速通道资质认证。今年5月30日,公司已向港交所递交招股书,拟在香港主板挂牌上市。
君圣泰医药(HighTideTherapeutics, Inc.)是一家全球一体化的新型生物技术公司 ,专注代谢性疾病、消化系统疾病等领域的重大未满足临床需求。公司立足源头创新,以患者的综合临床获益和整体健康改善为目标,开发First-in-Class、多功能、多靶点、多适应症的原创新药。
君圣泰医药以国际标准开发产品,在美国、澳大利亚、加拿大、中国等全球多个国家同步开展了十多项临床试验,产品的安全性和有效性获得多方验证,推动了传统天然产物的现代化和国际化,核心产品HTD1801已获得美国FDA授予的2项快速通道资格认定及1项孤儿药资格认定。
君圣泰医药的临床研究成果获得多家国际知名行业权威及国际知名学术期刊认可,从2019年起,公司连续多年将多项临床研究成果发布于世界权威肝脏病会议,并入选2021年美国肝病学会年会(AASLD)“The Best of The Liver Meeting” ;曾多次在欧洲肝脏研究学会(EASL)年会上展示重磅临床研究结果 。2020年,在Lipid in Health and Disease发表HTD1801在高脂血症患者中完成的2期临床试验数据 。2021年,Nature子刊Nature Communications在线发表HTD1801对非酒精性脂肪性肝炎(NASH)合并2型糖尿病(T2DM)患者的临床2期试验数据,并被主编选为“精选论文”(Featured Article)。2022年,HTD1801在成人原发性硬化性胆管炎(PSC)患者中完成的临床2期研究结果在American Journal of Gastroenterology发表。2023年,EASL大会上展示HTD1801显著降低NASH患者校正T1加权成像(cT1)的临床数据。
君圣泰医药自主研发的新药全部拥有100%全球知识产权,申请发明专利128项,专利授权覆盖中国、美国、欧洲、澳大利亚、新西兰、俄罗斯、新加坡、日本亚洲等全球主要国家和地区。基于自主知识产权,公司已研发出一条包含5款专利候选药物的管线,涵盖9种适应症,在全球推进多项中、后期临床试验。
在分子机理上,君圣泰医药的HTD1801具有标本兼治的特点,可以改善多条代谢通路、减少炎症、优化肠道菌群等,其设计理念与现有药物不同,深具创新性。本次公布的是一项随机、双盲、安慰剂对照的2期数据。
君圣泰医药发展历程很快,2011年-2016年:2011年公司设立,原创新药完成了创新分子临床前研究及专利申请,产品获得美国FDA孤儿药资格认定;2017年-2018年:君圣泰医药在美国、澳大利亚、加拿大等国家启动全球临床试验,核心产品获得美国FDA的2项快速通道资格认定,获2项中国“十三五重大新药创制”重大专项课题。 2019年-2020年:核心产品启动并完成多项全球临床2期试验,研究结果达到了主要终点及多个次要终点,产品的安全性和耐受性也获得了多方验证,且多个临床研究数据在国际知名肝病会议上展示。 2021年-2023年:推动多项产品临床中后期,超过四项2期临床研究取得了积极数据,公司从2019年至今,被认定为国家高新技术企业。
# 泰诺麦博生物:原创性天然全人源抗体类新药研发公司
4月14日,泰诺麦博生物(泰诺麦博)宣布新增康君资本、华金大道等股东,原有股东康哲药业继续增加投资,本次融资涉及近2亿元人民币。
泰诺麦博成立于2015年,总部位于珠海,专注于研发原创性天然全人源抗体类新药。该公司核心产品TNM002注射液是一款抗破伤风毒素单抗,即将递交新药上市申请。该公司在研产品主要为感染性疾病单抗。在具有差异化的疾病领域深耕,是泰诺麦博生物吸引投资的重要原因之一。
通过天然全人源单克隆抗体技术,泰诺麦博打造了稳固的多元化产品管线。 根据公司官网介绍,TNM001注射液是泰诺麦博重点产品,是我国潜在首款独立自主开发的长效全人源抗呼吸道合胞病毒(RSV)中和抗体药物,临床前研究结果显示其具有极高的中和能力,同时该抗体半衰期长,可覆盖整个RSV流行季。TNM002是泰诺麦博利用其天然全人源单克隆抗体研发综合技术平台HitmAb开发的重组抗破伤风毒素单抗药物,是全球潜在首款进入临床阶段的全人源抗破伤风毒素单抗新药,主要用于外伤暴露后破伤风的预防。
# 瑞风生物:基因编辑技术新药研发公司
4月28日,瑞风生物宣布完成数亿元Pre-B轮融资,本轮融资由越秀产业基金领投。本轮融资资金将用于加快推进地中海贫血药物的临床试验,持续推进后续基因编辑药物的研发及底层技术创新。
瑞风生物成立于2019年,总部位于广州。瑞风生物致力于新兴基因编辑药物的开发,在DNA和RNA水平的CRISPR/Cas和碱基编辑等多个方向的工具创新取得了阶段性成果。公司的β-地中海贫血基因编辑先导候选药物RM-001目前正在开展临床1期试验。
▲瑞风生物CAR-T产品管线(图片来源:公司官网)
根据公司介绍,团队成员既包括国际知名基因编辑领域科学家和具有国外临床机构科研经历的归国学者,也包括基因行业具有成功创业经验的创业者,是国际上最早应用基因编辑探索遗传疾病治疗的团队之一。其CEO梁峻彬获中山大学博士学位;作为连续创业者,梁博士曾联合创办安诺优达基因科技,此前曾任职于深圳华大基因和中科院广东省微生物研究所。
# 呈元科技:AI+合成肽药物研发公司
3月13日,呈元科技(Syneron Tech)宣布完成数千万美元Pre-A轮融资,本轮融资由联想创投和格力产投共同领投。
呈元科技成立于2022年4月,由创新工场塔尖孵化。该公司致力于通过AI加速合成肽类药物的研发,并搭建了AI+合成肽药物研发平台,实现了AI对于合成肽药物在其设计、筛选、合成、表征、优化等环节的全链条赋能,并已应用于多个潜在的“first-in-class”合成肽药物管线的研发。
创新工场董事长兼首席执行官李开复表示:“创新工场始终关注AI for Science科技交叉带来的技术突破和机遇。在Alphafold2蛋白质结构预测取得突破性进展的背景下,我们看到AI+蛋白方向出现‘序列—结构—功能’清晰的发展逻辑,AI在蛋白质设计领域展现出巨大的潜力。创新工场挖掘并协助从0到1塔尖孵化了呈元科技,公司在成立短短一年内已经搭建起交叉融合的国际化团队,期待呈元科技一步步成为全球领先的AI制药公司。”
# 达石药业:创新型抗体药物研发公司
1月20日,达石药业宣布完成超亿元B轮融资首关,由广东粤财控股旗下的中银粤财生物医药基金领投。根据达石药业新闻稿,本次所筹资金将用于推进公司临床研发、产品管线拓展、人才团队建设等。
达石药业成立于2018年,总部位于广东中山,是一家专注于创新型抗体药物研发的科技公司。加上早期药物发现品种,该公司共有多个新药研发项目在研。其中, 该公司靶向神经生长因子(NGF)的人源化重组单克隆抗体药物DS002已进入2期临床,另有多款针对疼痛或肿瘤并发症的抗体药物也正陆续进入临床阶段。
公开资料显示,DS002是达石药业自主研发、序列全新的一种靶向神经生长因子(NGF)的人源化重组单克隆抗体药物。在人体出现因受伤、炎症引起的疼痛或慢性疼痛时,NGF的水平也会相应上升。研究显示,通过选择性抑制NGF,可能有助于阻断肌肉、皮肤和器官产生的疼痛信号进入脊髓和大脑。
此前,DS002已在临床前研究中显示很好的安全性,在多种动物痛觉模型中也有很好的镇痛效果,可以实现每两个月用药一次的超长效果。值得一提的是,在作用机理上,DS002这一新作用机制与阿片类药物和包括非甾体类抗炎药(NSAIDs)在内的其它镇痛药完全不同,因此不会有成瘾性的风险。
# 瑞吉生物:mRNA药物研发公司
1月6日, 瑞吉生物完成亿元Pre-B轮融资,本轮融资由前海沃盈领投,包括红杉中国在内的其他原有股东全部继续跟投。本轮资金主要用于推进公司在研管线临床试验及产业化建设。
瑞吉生物成立于2019年,总部位于深圳,致力于开发mRNA等核酸类生物医学产品及治疗方法,拥有mRNA技术领域全技术平台,可根据临床及成药性需求,设计开发mRNA药物。公司管线涵盖传染病疫苗、肿瘤免疫治疗和蛋白替代疗法。2022年6月以来,由瑞吉生物主导研发的冻干型新冠mRNA疫苗(奥密克戎株)RH109分别在菲律宾、新西兰和中国香港获得临床批件,随后不久此款疫苗被选中开展专项临床研究
早在2021年初,红杉中国就以早期医疗投资者的身份,独家参与了瑞吉生物的A轮融资。红杉中国合伙人杨云霞表示,对于瑞吉生物的投资,既是红杉作为专业医疗投资机构在核酸药物这样一个极为前沿、细分的技术领域中投资研究能力的综合体现,更是助力优秀公司成长、为全社会做贡献的宝贵机会。
# Wondercel Therapeutics:细胞疗法研发公司
2月10日,Wondercel Therapeutics完成近亿元天使轮融资,本轮融资由元生创投投资。
Wondercel Therapeutics由南京传奇生物前首席科学官范晓虎博士创立。范博士在南京传奇生物建立了优秀的科研团队,其自主开发的靶向BCMA的双表位CAR-T产品西达基奥仑塞注射液于2022年在美国,欧盟以及日本获得上市批准。西达基奥仑塞注射液是属于BCMA靶点创新药的潜在“best-in-class”产品。范博士被国际媒体Endpoints News评为“全球Top 20最有影响力的药物研发领袖”。
西达基奥仑塞注射液的成功验证了范博士在细胞治疗领域的创新和科研转化能力,他将继续致力于探索解决细胞药物存在的现有不足,开发更安全更经济下一代免疫细胞治疗技术,从而释放人源免疫细胞在肿瘤治疗、器官移植、自身免疫性疾病等治疗领域的无限潜能。
推广
-推广-
凡本网注明 “来源:XXX(非本网)” 的作品,均转载自其它媒体,转载目的在于传递更多信息,并不代表本网赞同其观点和对其真实性负责。
上一篇: 农发行准格尔旗支行提前实现粮食市场化收购贷款“双结零”